
导语
肺癌作为全球发病率和死亡率稳居前三的恶性肿瘤,一直以来备受关注,新辅助治疗为局晚期肺癌患者带来了更多的根治机会。免疫治疗在肺癌新辅助治疗中的应用价值已经得到了临床研究的初步证实,但前期临床研究显示免疫新辅助治疗仍然存在pCR率偏低、影像学疗效评估与病理缓解一致性偏低等问题,需要进一步尝试通过免疫联合治疗提高新辅pCR率,同时探究ctDNA MRD监测技术能否更好的评估免疫新辅疗效。
中国医学科学院肿瘤医院高树庚教授团队开展了卡瑞利珠单抗联合阿帕替尼的肺癌新辅助临床研究,证实了免疫联合抗血管治疗具有较好的新辅助治疗疗效,同时在研究中采用ctDNA MRD监测技术,证实了ctDNA MRD监测在新辅助疗效评估中的价值。研究成果发表在Journal of Thoracic Oncology(IF=20.131)。
研究亮点
1、首次将卡瑞利珠单抗联合阿帕替尼方案应用于可切除IIA-IIIB期NSCLC新辅助治疗中,并取得良好临床结果:毒副作用可控, 57%的手术患者达到主要病理缓解(MPR),23%的患者达到pCR;
2、进一步证实ctDNA能早期预测接受新辅助治疗的可手术NSCLC患者的病理反应和术后疾病复发。
研究设计
这是一项前瞻性、单臂Ⅱ期临床试验,筛选纳入年龄18岁至70岁,经组织学证实可切除ⅡA-ⅢB期(ⅢB期仅限T3N2M0)的NSCLC患者。主要终点是疗效分析集(EAS)中的MPR率(定义为MPR患者的比例);次要终点包括pCR率、客观缓解率(ORR)、疾病控制率(DCR)、无病生存期(DFS)、无事件生存期(EFS)和安全性;还探讨了影像学、组织和血液生物标志物与疗效之间的相关性。
研究结果
卡瑞利珠单抗联合阿帕替尼方案在可切除NSCLC新辅助治疗中具有良好应用前景
2020年11月9日至2022年2月16日,研究共筛选了91例患者,其中78例患者纳入分析。在这78例患者中,40例(51%)为Ⅲ期患者,其中11例(14%)为可切除的ⅢB期。经病理确认,鳞癌59例(76%),N2淋巴结受累27例(35%)。所有患者均接受卡瑞利珠单抗联合阿帕替尼方案治疗,共有65例(83%)行手术切除,其中37例(57%)行胸腔镜手术(VATS),另有3例(5%)患者在VATS术中转为开胸手术。65例患者(100%)均达到R0手术切除。7例(11%)患者出现手术并发症,其中肺炎3例(5%)。
新辅助治疗后,65例达到R0手术切除的患者中,2例(3%)达到影像学CR,32例(49%)PR,ORR为52%(95% CI 40%~65%)。65例手术切除患者中,37例(57%,95 %CI 44%~69%)达到MPR,其中3例(25%,95%CI 5%~57%)为肺腺癌,34例(64%,95% CI 50%~77%)为鳞状细胞NSCLC;15例(23%,95% CI 14%~35%)达到pCR,均为鳞癌(图1)。在78例入组患者的全分析集(FAS)中,37例(47%,95% CI 36%~59%)达到MPR,15例(19%,95% CI 11%~30%)达到pCR。
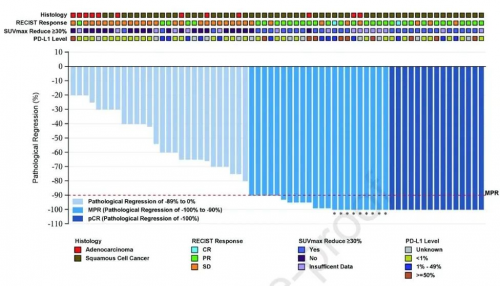
图1. 新辅助治疗后手术切除患者病理缓解的瀑布图
PET-CT与接受新辅助免疫治疗的可手术NSCLC患者的病理反应显著相关
78例入组患者中,61例(78%)术前进行PET-CT评估。结果显示,26例(52%)存在部分代谢反应(PMR),1例(2%)存在完全代谢反应(CMR),总计25例(93%,25/27)存在MPR。最大平均摄取值(SUVmax)下降与病理缓解(R=0.619,p<0.0001)之间存在显著相关性。根据ROC曲线,SUVmax下降率为-32%,预测MPR的敏感度(93%)和特异度(91%)最高(图2)。
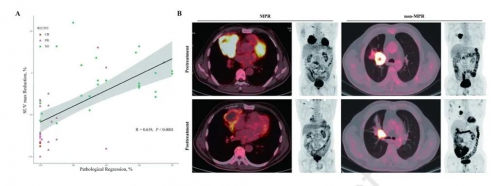
图2. SUVmax下降与病理缓解的相关性
ctDNA状态可提示NSCLC患者新辅助治疗后病理反应和术后疾病复发
对65例接受手术治疗的患者基线组织样本进行高通量测序,如图3所示:KRAS(50%)、TP53(25%)和ARID1B(17%)是肺腺癌中最常见的突变基因;在鳞状细胞癌中,TP53(85%)和Lrp1B(47%)最常见。进一步分析肿瘤突变负荷(TMB)与治疗疗效的相关性,高TMB患者具有更好的MPR和pCR倾向性,但并无显著的统计学差异(p=0.1691和p=0.3847)。
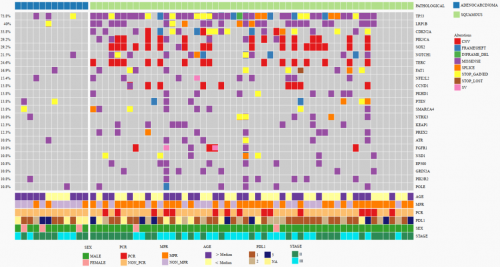
图3. 基线组织突变图谱
同时,为了进一步评估MRD状态对于新辅助治疗的疗效预测价值,研究比较了不同时间点 (治疗前[TP0]、新辅助治疗第2周期前[TP1]、第3周期前[TP2]和手术前[TP3])的ctDNA浓度和ctDNA动态变化趋势(图4)。随着新辅助治疗的进行,未达到pCR/MPR的患者术前ctDNA浓度高于达到pCR/MPR的患者;就ctDNA清零率而言,与未达到MPR/pCR的患者相比,MPR/pCR患者在TP2和TP3时有更好的ctDNA清零率(图5)。
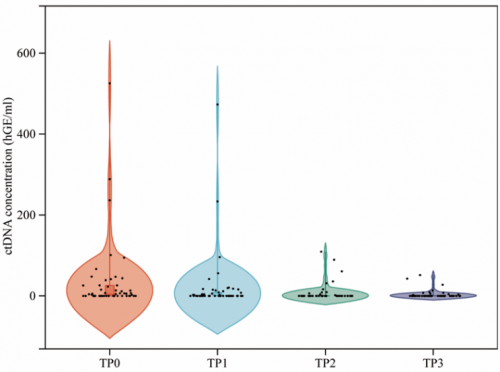
图4. 四个不同时间点的ctDNA浓度
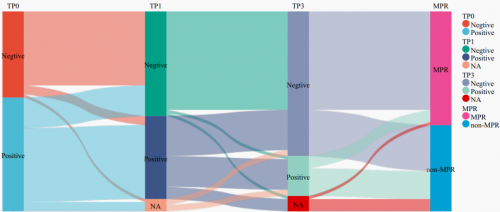
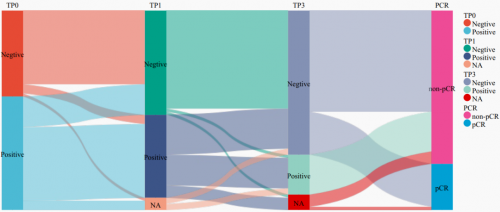
图5. 新辅助治疗期间ctDNA动态变化
结语
在ⅡA-ⅢB期可切除NSCLC患者的新辅助治疗中,卡瑞利珠单抗联合阿帕替尼方案显示出良好的疗效和可控的不良反应(MPR率为57%、pCR率23%),或可成为NSCLC新辅助治疗的潜在治疗选择。
PET-CT能较好地预测新辅免疫治疗疗效, SUVmax降低与病理缓解之间存在显著相关性,将SUVmax下降的阈值设定为-32%,预测达到病理缓解的敏感性和特异性分别为91%和93%。
基于ctDNA的MRD监测能早期预测接受新辅助免疫联合抗血管治疗的可手术NSCLC患者的病理反应和术后疾病复发。ctDNA MRD状态可能是病理缓解的早期预测因素。
本研究使用了世和基因泛实体瘤围术期MRD监测产品术宁。
参考文献
[1] Zhao J, Zhao L, Guo W, et al. Efficacy, Safety, and Biomarker Analysis of Neoadjuvant Camrelizumab and Apatinib in Patients with Resectable Non-Small-Cell Lung Cancer: A Phase 2 Clinical Trial[J]. Journal of Thoracic Oncology, 2023.
 健康教育网
健康教育网












